新闻中心
.png)
[ 基金项目 ] 中央级公益性科研院所基本科研业务费专项( ZZ14-YQ-05 6 , ZZ17-ND-10-13 )
[ 摘要 ] 目的:运用化学蛋白质组学技术筛选白藜芦醇发挥抗肥胖作用的直接靶标蛋白,从线粒体功能调控、脂肪棕色化及炎症抑制角度,系统探究其抑制脂肪细胞脂质积累的分子机制,为肥胖及相关代谢性疾病 的防治提供新的靶点与实验依据。方法:以3T3-L1小鼠前脂肪细胞为研究对象,采用CCK-8法检测细胞存活率,确定白藜芦醇的安全有效剂量(7.5、15、30μmol/L);诱导分化为成熟脂肪细胞后分为空白组(DMSO处理)和白藜芦醇给药组(7.5、15、30μmol/ L),各给药组均作用48h ;通过油红O染色结合甘油三酯(TG)定量检测,观察白藜芦醇对脂肪细胞脂质积累的影响;利用碘代乙酰胺炔烃(IAA-P)化学蛋白质组学联合高分辨率质谱对自藜芦醇进行靶标蛋白“垂钓”,并采用细胞热转变分析(CETSA)结合Western blot验证靶标蛋白;通过Western blot检测脂肪棕色化标志性蛋白过氧化物酶体增殖物激活受体γ共激活因子1α(PGC-1α)、线粒体解偶联蛋白1(UCP1)及靶标蛋白NDUFS8、HMGB1的表达,采用增强型ATP检测试剂盒测定细胞ATP含量,结合Mito-tracker green 染色观察线粒体数目,分析白藜芦醇对线粒体功能的调控作用;运用ELISA检测细胞上清中炎症因子TNF-α水平,探究白藜芦醇对脂肪炎症的改善效果。结果:与空白组比较,Res显示在 7.5~30μmol/L范围内安全有效,对细胞活性无显著性影响;与空白组比较,Res不同浓度给药组,显著降低3T3-L1脂肪细胞脂质积累 。靶标“垂钓”结果表明,NDUFS8/HMGB1为Res发挥药理活性的重要靶标蛋白。进一步对Res靶标蛋白进行确证,结果表明 Res 不影响靶标蛋白HMGB1 表达水平,可显著增加 NUDFS8 靶标蛋白表达水平。 CETSA 实验表明,与空白组比较 Res 可增加靶标蛋白 HMGB1 以及 NDUFS8 的热稳定性。作用机制研究表明,Res 可促进 3T3-L1 脂肪细胞棕色化,与空白组比较 Res 给药 组剂量依赖性促进线粒体功能重要蛋白( UCP1 、 PGC-1 α ) 表达,促进 ATP 合成,改善线粒体功能。同时,与空白组比较 Res 给药组抑制细胞炎症因子 TNF- α 的分泌,改善炎症反应。 结论: NDUFS8/HMGB1 是 Res 发挥药理活性的重要靶标蛋白, Res 通过靶向 NDUFS8 调控线粒体功能促进脂肪棕色化,Res 通过靶向 HMGB1 抑制 TNF- α 炎症通路的激活,抑制脂质积累进而改善肥胖。[ 关键词 ] 化学蛋白质组学;白藜芦醇; 脂质积累; NDUFS8 ; HMGB1
[ 中图分类号 ] R282;R259;R285 [ 文献标识码 ] A
[doi] 10.13422/j.cnki.syfjx.20 260501
01 研究背景
2025 年初国家卫健委发布《体重管理指导原则( 2024 年版)》,明确 BMI (body mass i ndex) 指数 ( ≥28 为肥胖, 目前我国超半数成年人超重或肥胖,远高于世卫组织的 37% ,预计 2030 年成人率将分别超 70.5% 。肥胖是 2 型糖尿病、冠心病等代谢性疾病的重要危险因素,临床亟需安全有效的减肥药物,而国家“ 体重管理年 ”行动的启动,也为肥胖科学干预提出了新要求。中医对肥胖的认识历史悠久,以“ 痰 ”为核心病机之一。《黄帝内经》中记载 “ 肥贵人则膏粱之疾也 ”,《石室秘录》有“ 肥人多痰 ”之说,过食肥甘或脾胃运化失常,致痰湿内生、水谷精微布散失常,进而引发脂肪细胞功能障碍与脂肪炎症 。哺乳动物脂肪细胞分白色( WAT )和棕色( BAT )两类:白色脂肪以单房大脂滴储脂,线粒体稀少;棕色脂肪含多房小脂滴,线粒体丰富,其内膜高表达的UCP1可激活解耦联通道,阻断氧化磷酸化,将质子势能以热能形式释放。棕色脂肪可在寒冷时产热维持体温,曾被认为仅存在于啮齿类动物和人类新生儿。后续研究发现,成年人体颈部、锁骨区域的棕色 脂肪含量及活性与BMI呈负相关;且白色脂肪在寒冷、激素等刺激下,会向兼具白、棕脂肪特性的米色脂肪转化,即脂肪棕色化,该过程能提升脂肪耗氧与产热,成为肥胖治疗的研究焦点。中医药在干预肥胖具有独特优势,其作用温和持久,不良反应小。天然产物是中药药效的物质基础,白藜芦醇( Res )作为一种典型的多酚类天然产物,广泛存在于葡萄、花生、桑葚、虎杖等 70 多种植物。白藜芦醇具有抗炎、抗癌、心脏保护、神经保护、改善糖代谢异常和胰岛素抵抗等多重药理活性。现代研究表明, Res 可作为沉寂信息调节因子( SIRT1 )的激活剂,对过氧化物酶体增殖物激活受体 γ 辅激活因子 1 ( PGC-1 α ) 进行去乙酰化修饰,增强线粒体功能。 Res 可以激活 AMPK 信号通路,调节生物能量代谢。同时,Res 还可以刺激瘦素( leptin )等脂肪因子及鸢尾素( FNDC5/irisin )等肌肉因子的生成,提高机体代谢灵活性,改善胰岛素抵抗。 Res 被证实可预防癌症、代谢性疾病等多种病症,参与自噬、抗炎等诸多生理过程 。目前,Res 的直接作用靶标蛋白是什么,该靶点与哪些下游蛋白发生相互作用及其调控机制仍有待阐明。天然产物可通过多个活性中心,协同调控相互关联的分子与通路网络,发挥多靶点效应。活性蛋白质谱分析( ABPP )技术能通过点击化学高效捕获鉴定药物靶蛋白,其靶点阐释可为天然产物开发、创新药研发提供关键支撑。本研究采用诱导分化成熟的 3T3-L1 脂肪细胞模型,结合基于碘代乙酰胺炔烃( IAA-P )化学蛋白质组学技术,利用高分辨率蛋白质谱,对 Res 进行靶标“ 垂钓 ”, 并通过细胞热转变分析( CETSA )-蛋白免疫印迹法( Western blot )对 Res 靶标蛋白进行确证,进而阐明 Res 促进脂肪棕色化、改善脂肪炎症的分子机制,为肥胖及相关代谢性疾病的防治提供新策略。
02 材料
1.1 细胞
小鼠前脂肪细胞 3T3-L1 细 胞株,于武汉武汉普诺赛生命科技有限公司购得(货号:CL-0006 ),取对数期细胞用于后续实验。
1.2 药品
白藜芦醇(上海源叶生物科技有限公司,纯度大于 98% ,批号 38963-95-0 ),用 DMSO 配置,置于 4 ℃ 冰箱冷藏备用。
1.3 试剂
STING 激活剂 ADU-S100 、胰岛素(美国 MedChe mExpress 公司,货号分别为 HY-12885 、 HY- P0035 ); 3-异丁基-1-甲基黄嘌呤(IBMX)、地塞米松、三乙胺( TEA )、 1-(3- 二甲氨基丙基 )-3- 乙基碳二亚 胺盐酸盐( EDCI )、 1- 羟基苯并三氮唑( HOBt )、二氯甲烷( CH₂Cl₂ )、 硫酸铜、二甲基试剂标记、二硫苏 糖醇( DTT )、碘乙酰胺( IAA )( 美国 Sigma-Aldrich 公司,货号分别为 I5879 、 D4902 、 TX1200 、 39391 、 54802 、 1601441 、 C1297 、 215511 、 3860-OP 、 I3750 ); 胰酶(中国北京索莱宝科技有限公司 ,货号 T1300 );青霉素 - 链霉素双抗、 0.25% 胰蛋白酶消化液(美国 Thermo Fisher Scientific 公司 Gibco 分公司,货号分 别为 2441838 、 25200072 ); 胎牛血清(美国 Corning 公司,货 号 35-081-CV ); 细胞计数试剂盒 -8 ( CCK-8 ,中国大连美仑生物技术有限公司,货号 MA0218-JUN-04J ); 噻唑蓝( MTT )试剂盒(中国上海贝博生物科技 有限公司,货号 BB-4201 ); Triton X-100 、蛋白酶抑制剂、BCA检测盒、考马斯亮蓝( CBB )染色、油红 O 染色试剂盒、 Mito-Tracker Gre en 、增强型 ATP 检测试剂盒(中国碧云天生物技术有限公司,货号分别为 P0096 、 P1005 、 P0011 、 P0017 、 C0157S 、 C1048 、 S0027 ); ECL 发光液(美国 Engibody 公司,货号 IF6748 ); 一抗 UCP1 、 NDUFS8 、 HMGB1 (美国 Proteintech 公司,货号分别为 23673-1-AP 、 25172-1-AP 、 1 0829-1-AP );一抗 PGC-1α (美国 Cell Signaling Technology 公司,货号 2178S ); 一抗 GAPDH 、 cGAS 、 STING 、二抗 HRP (美国 Abcam 公司,货号分别为 ab22555 、 ab302617 、 ab239074 、 ab40742 ); 二 抗 Rabbit 、 Mouse (中国武汉正能生物科技有限公司,货号分别为550048 、511103); 白细胞介素 -1β ( IL-1β )、 白细胞介素 -6 ( IL- 6 )、白细胞介素 -15 ( IL-15 )、白细胞介素 -23 ( IL-23 )、干扰素 -γ ( IFN-γ ) ELISA 试剂盒(中国武汉伊莱瑞特生物科技股份有限公司,货号分别为 E-EL-H0149 、 EHSELH 0003 、 EELH0222 、 EELH0107 、 EHSELH0007 );肿瘤坏死因子 α ( TNF -α ) 测试盒(中国上海华英生物科技有限公司,货号 HY -H0019 ); 甘油三酯( TG ) 测试盒(中国南京建成生物工程研究所,货号 A110-1-1 ); 3-羟丙基三氮基甲基三胺( TBTA )、三(2- 羧乙基)膦盐酸盐( TCEP )、羧基四甲基罗丹明( TAMRA )、生物素叠氮磁珠( biotin-N3 )( 美国 Click Chemistry Tools 公司,货号分别为 CCT-1010 、 QBD-10014 、 CCT-TA108 、 QBD-10202 ) 。 所有操作按照试剂说明书进行。
1.4 仪器
LAMBDA365 + 型酶标仪 ( 美国 PerkinElmer 公司 ) , Mini-PROTEAN® Tet ra 型电泳系统 ( 美国 Biorad 公司 ) , Mini Trans-Blot® Module 型 WB 转膜仪 ( 美国 Biorad 公司 ) , Azure 600 型可见荧光 Western Blot 成像系统 ( 美国 Azure Biosystems 公司 ) , Orbitrap Fusion LumosTribrid 型 LC-MS/MS 串联质谱 ( 美国 Thermo Fisher 公司 ) , Andor Dragonfly 2000 高速转盘共聚焦显微镜(英国 Andor Technolog y Ltd. 公司)。
03 方法
2.1 细胞系及细胞培养
来自 ATCC 的 3T3-L1 小鼠前脂肪细胞在在 37℃ 、 5% CO2 的培养箱中培育,使用含有 10% 小牛血清 (Gibco) 和 1%P/S 的 DMEM 培养,等细胞融合后,更换为分化培养基(含 10% 胎牛血清、1μmol/L 地塞米松、 0.5mmol 异丁基甲基黄嘌呤、 5μg/mL胰岛素的 DMEM )处理 2 d 。此后,细胞在含 10% 胎牛血清和 5μg/mL胰岛素的 DMEM 中继续培养 6 d ,隔天更换 1 次培养液,细胞完全分化为成熟脂肪细胞需第 8 天,进行后续实验。
2.2 油红 O 染色
3T3-L1 细胞以每孔 1×105 个细胞密度接种于 6 孔板中,按上述培养方案得到完全分化的脂肪细胞后进行分组,即空白组 (DMSO) 与 Res 给药组(Res,7.5、15、30μmol/L)。加入或不加入Res孵育48h后,根据试剂盒说明书进行油红 O 染色,倒置显微镜下观察脂肪积累情况。
2.3 CCK-8 检测细胞存活率
CCK-8 法筛选白藜芦醇最佳治疗剂量,3T3-L1细胞以105个/mL孔细胞密度接种于96孔板,进行上述分组处理,每组 6 个复孔,加或不加 Res 孵育 48 h 后,加入含有 10%C CK-8 试剂的 DMEM ,37℃ 孵育 30~60 min ,酶标仪 450 nm 测 吸光度 A 值确定细胞存活率 。细胞相对存活率 (%)=(As−A0)/(Ac−A0)·10 0% 。
2.4 TG 含量检测
3T3-L1 细胞以每孔 105个/mL个细胞密度接种于 6 孔板中,按上述培养方案得到完全分化的脂肪细胞,并进行上述分组,根据 TG 试剂盒说明书测定细胞内 TG 含量,并通过 BCA 蛋白定量分析测定 每组细胞蛋白浓度从而校正细胞内 TG 水平。
2.5 Western blot 检测
如上所述,加或不加 Res 处理细胞后裂解细胞,加入 RIPA 裂解液,用细胞刮刀收集细胞,4 ℃ ,15000 r/min ,30 min(离心半径 8 cm )收集上清液制备样品, BCA 蛋白定量分析测定总蛋白浓度。通过 SDS-PAGE 电泳分离,将蛋白转移到聚偏氟乙烯 (PVDF) 膜上,在 5% 脱脂牛奶中封闭 2h ,与一抗(1 :1000)在 4℃ 孵育过夜后选用相应二抗(1 :5000 )室温反应 2h ,最后用酶联化学发光试剂检测蛋白条带。结果采用 ImageJ 软件进行灰度值分析。
2.6 ABPP 鉴定蛋白靶点
按照上述细胞培养方案提取 3T3-L1 细胞裂解液,加或不加Res 、去硫代碘乙酰胺 (DBIA) 探针,使用 DTT 和 IAA 还原并烷化半胱氨酸残基,用胰酶将蛋白质消化成多肽,进行二甲基标记后通过链亲和素珠富集生物素化蛋白,最后将肽段洗脱后过柱除盐,进行 LC-MS/MS 分析。通过比较探针组和竞争组,发现可能与 Res 结合的蛋白。
2.7 ATP 含量检测
3T3-L1 细胞以每孔 105 个/mL个细胞密度接种于 6 孔板中,按照上述分化培养方案获得完全分化的脂肪细胞,加或不加 Res 孵育 48h 后,收集细胞进行裂解。根据试剂盒说明书,进行细胞 ATP 含 量检测。此外,以蛋白含量作为参考值对 ATP 水平进行标准化,与空白组进行比较。
2.8 CETSA 验证
3T3-L1 细胞以每孔 2.5×105个/mL 细胞密度接种于 1 0 cm 皿中,等细胞密度达到 80%~90% 后,使用 RIPA 裂解液并刮取细胞, 4 ℃ 、 15 000 r/min 、离心 30min ,收集上清液即为细胞总蛋白。将上清均分为两组,对照组加入 DMSO ,药物组加入 Res ( 30 μmol/L),室温震荡孵育 1 h 。反应结束后,每组平均分成八份,加入 PCR 小管中,两组分别在 37 、 42 、 47 、 52 、 57 、 62 、 67 、 72℃ 下加热 6min ,反应结束后, 20000g 、 4℃ 、离心 20min ,收取等量上清,加入 1xloading buffer ,95℃ 煮样 10min 后进行 Western blot 实验。结果采用 ImageJ 软件进行灰度分析。
2.9 Mito-tracker 染色
3T3-L1 细胞以每孔105 个/mL个的细胞密度接种于四分皿中,如上所述,获得完全分 化的脂肪细胞后分组,加或不加 Rse 孵育 48h 后,去除细胞培养液,使用 37 ℃ 预温育的工作液(含 100nmol/L Mito-Tracker Green 储存液、1μg/mL Hoechst 33342 ),与细胞 37℃ 避光孵育 30 min ,用激光共聚焦显微镜在490 、450nm 波长下进行线粒体及细胞核观察。
2.10 ELISA 检测炎症因子 TNF- α
3T3-L1 细胞接种于 6 孔板中,按照上述分化培养方案获得完全分化的脂肪细胞,加或不加 Res 孵育 48h 后,收集细胞上清 200μL,按照 ELISA 试剂盒说明书进行操作。
2.11 统计学方法
采用 GraPhPad Prism 9.5.1 软件进行数据分析,实验所得计量资料用 × ± s 表示, 两组间数据比较采用 Student's t 分析,多组间数据比较采用单因素方差分析( ANO VA ),P<0.05 为差异具有统计学意义。
04 结果
3.1 白藜芦醇( Res )抑制脂质积累
油红 O 染色结果表明,空白组细胞中出现大量脂滴,与空白组比较, Res 给药组细胞中脂滴含量显著减少,表明 Res 可显著抑肪细胞的脂质累积,见图 1 。
.png)
图 1 白藜芦醇( Res )抑制脂质积累油红 O 染色结果
细胞活力检测结果表明,与正常组比较,Res 不同浓度给药组均对细胞活力无显著影响,同时,对不同浓度 Res 给药组细胞进行总甘油三酯( TG )含量进行检测,结果表明,3T3-L1 脂肪细胞 TG 含量在 Res 作用下,与空白组比较,各给药组 TG 含量呈剂量依赖性降低(P<0.05 ,P<0.01),见表 1 。为进一步研究 Res 改善肥胖作用机制,选取7.5、15、30μmol/L进行后续实验。
.png) 表 1 Res 剂量依赖性安全有效降低 3T3-L1 脂肪细胞总甘油三酯含量( × ±s, n= 6 )注:与空白组比较, 2)P <0.01 , 1)P <0.05 ,下表同。
表 1 Res 剂量依赖性安全有效降低 3T3-L1 脂肪细胞总甘油三酯含量( × ±s, n= 6 )注:与空白组比较, 2)P <0.01 , 1)P <0.05 ,下表同。
3.2 基于化学蛋白质组学方法进行 Res 靶标标蛋白分析
为进一步研究白藜芦醇靶标蛋白,使用基于碘代乙酰胺炔烃( IAA-P )化学蛋白质组学对 Res 进行药物靶标“垂钓”,IAA-P 这种基于活性的半胱氨酸 探针是目前用于半胱氨酸相关蛋白的药物靶标分析中,使用最广泛的探针,“钓”取目标蛋白,然后通过分子探针的标签集团对靶标蛋白进行分离和生物质谱鉴定(Pull-d own/LC-MS), 从而达到准确鉴定药物分子作用靶标的目的,具体实验原理及流程见图 2A 。化学蛋白质组学结果显示, IAA-P 可与 Res 竞争结合药物靶标蛋白,且呈剂量依赖性,Res 在 400μmol/L达到最大竞争效应,见图 2B 。因此,IAA-P 在 3T3-L1 细胞上与 Res 具有等效性。基于 IAA-P 开展的 Res 药物靶标“垂钓”结果显示,HMGB1 ,NDUFS8 显示出显著潜力,是 Res 发挥药 理活性的重要靶标蛋白,见图 2C 。GO (Gene Ontology) 通路富集分析结果显示,靶标蛋白 HMGB1 通过调节细胞炎症反应, NDUFS8 通过调节氧化还原稳态、细胞氧化磷酸化,二者相互作用共同参与脂质代谢发挥 Res 改善肥胖的药理活性,见图 2D 。蛋白质 - 蛋白质互作( PPI )网络结果显示,HMGB1 可正向调节 TNF- α 炎症通路、炎症模块的核心枢纽,HMGB1 水平与衰老、慢性低度炎症呈正相关; NDUFS8 调控氧化磷酸化能量代谢模块,NDUFS8 直接参与电子传递和质子泵出,改善 NDUFS8 功能可恢复氧化磷酸化效率,增加 ATP 产生,缓解代谢应激,结果见图 2E 。以上靶标蛋白机制互补,同时纠正能量代谢障碍和慢性炎症。
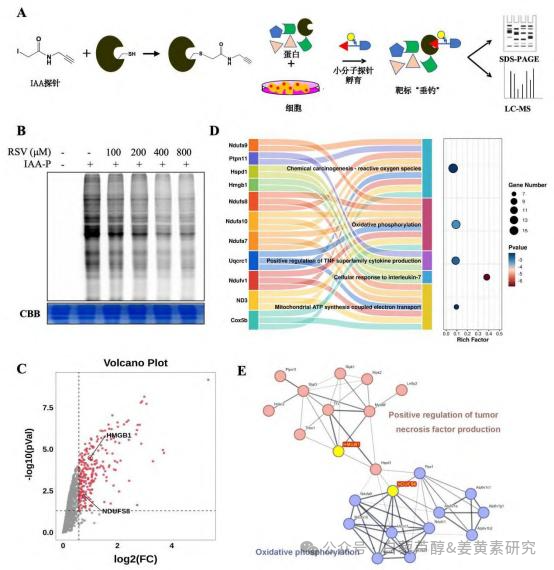
注: A. 基于 IAA-P 化学蛋白质组学实验流程; B.IAA-P 探针标记, CBB 考马斯亮蓝染色; C.LC-MS/MS 鉴定 Res 潜在靶标蛋白; D.GO 通路分析; E. 蛋白质 - 蛋白质互作( PPI )网络分析
图 2 基于蛋白质组学技术对 Res 进行靶标蛋白分析
3.3 Res 靶标蛋白确证
对 Res 蛋白进行确证, Res 可促进 NDUFS8 蛋白表达升高,而针对另一个重要靶标蛋白 HMGB1 ,并未影响其表达水平,见图 3A 、表 2 。细胞热转变分析实验结果表明,随温度升高,与空白组比较 Res 与靶标蛋白 HMGB1 以及 NDUFS8 的热稳定性增加(P < 0.05 ,P <0.01 ),见图 3B ,证实了 Res 与靶标蛋白之间的直接相互作用。
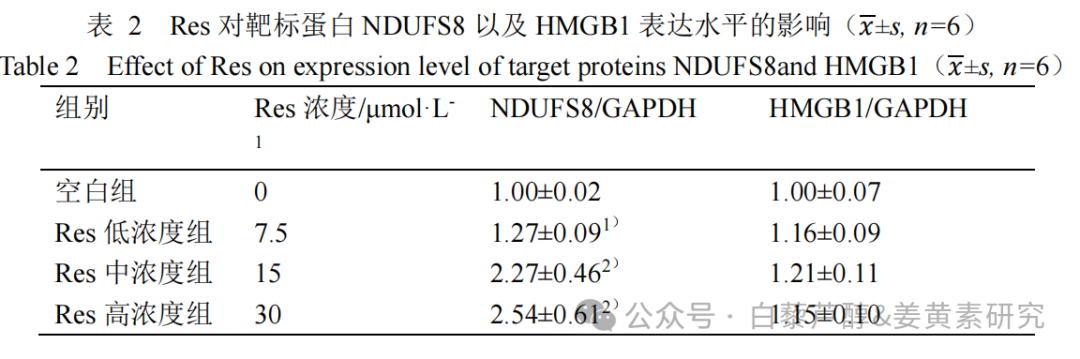
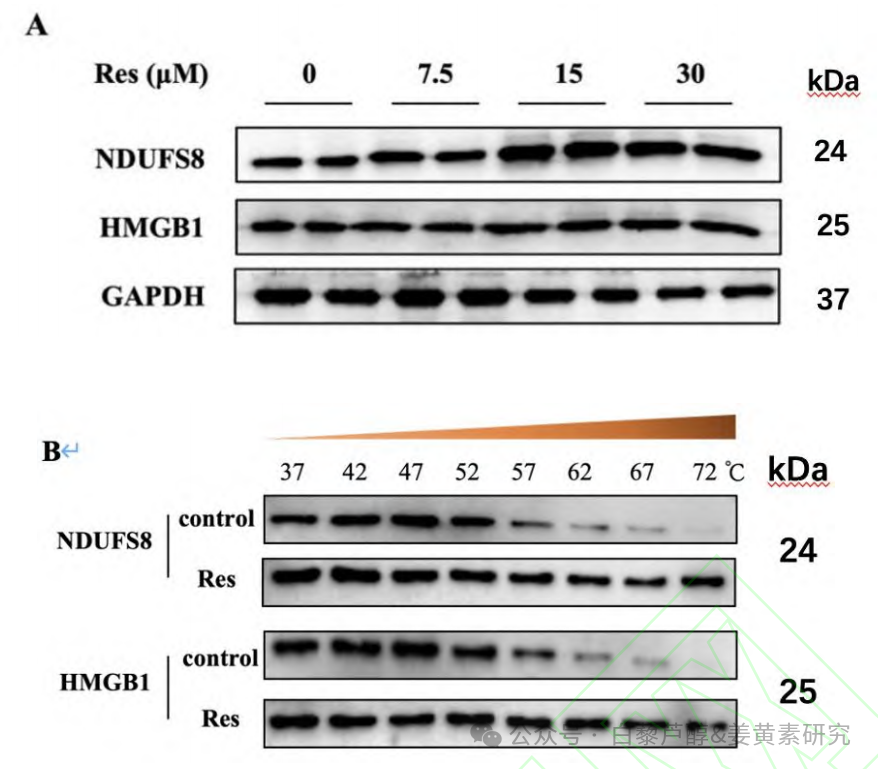
A.Western blot 检测 Res 对靶标蛋白 NDUFS8, ,HMGB1 表达水平的影响; B.CETSA-WB 检测靶标蛋白 NDUFS8 及 HMGB1 热稳定性
图 3. Res 靶标蛋白确证
3.4 Res 促进脂肪棕色化发挥降脂活性
线粒体作为 ATP 合成的重要场所,ATP 合成能力也是脂肪棕色化的重要指征, Res 可促进 ATP 合成,与空白组比较, Res 给药组 3T3-L1 脂肪细胞 ATP 含量增加( P <0.05 , P <0.01 ), 见表 3 。与空白组比较, Res 给药组线粒体染色荧光强度显著增强( P <0.05 , P <0.01 ), Res 促进线粒体合成,增加线粒体数目,见图 4A 。与空白组比较 , Res 给药组显著增强 3T3-L1 脂肪细胞棕色化指征蛋白 UCP1 、 PGC-1 α 表达,促进脂肪棕色化抑制脂肪细胞脂质积蓄( P <0.05, P <0.01 ), 见图 4B 、表 4 。上述 结果表明 Res 通过靶向 NUDFS8 促进促进脂肪棕色化,线粒体生物合成,发挥药理活性。

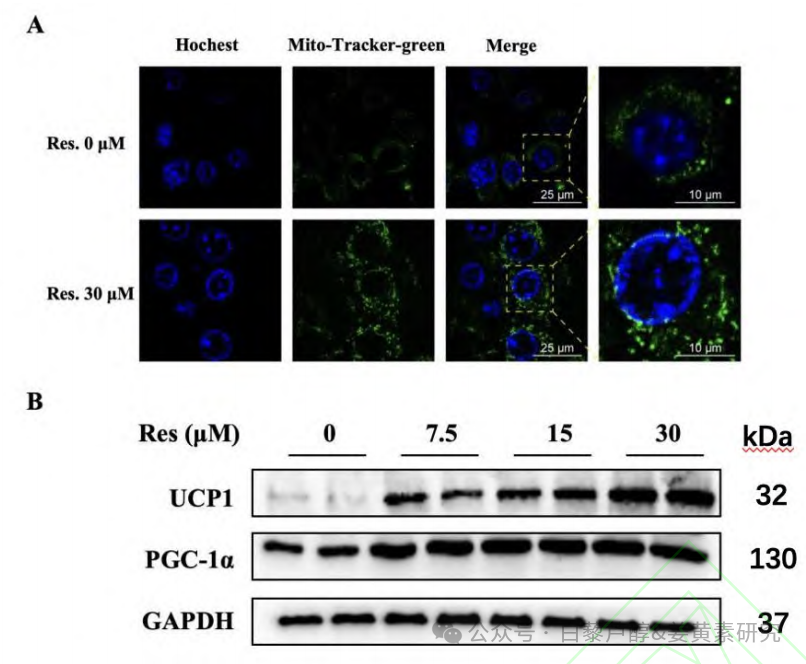
注: A.Mito-tracker green 检测线粒 体数量; B.Western-blot 检测脂肪棕色化相关蛋白 PGC-1 α 、 UCP1 的表达图
图 4 Res 促进脂肪棕色化,促进 线粒体生物合成

3.5 Res 改善脂肪炎症发挥降脂活性
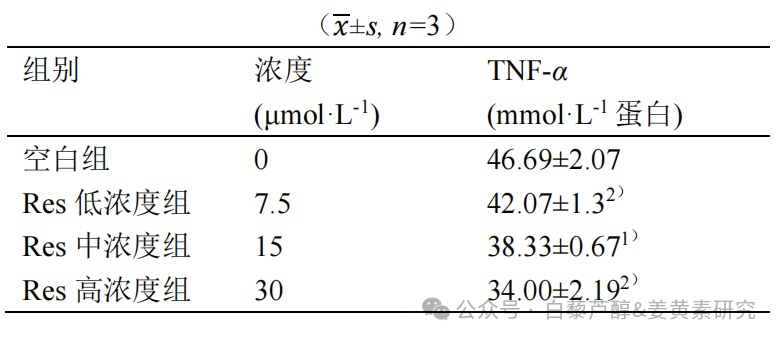
与空白组比较, Res 给药组可剂量依赖性降低炎症因子 TNF - α水平( P <0.05 ,P <0.01 ),见表 5 。上述结果表明,与空白组比较, Res 通过靶向 HMGB1 ,特异性抑制 TNF- α 信号通路, Res 能够有效缓解脂肪炎症,进而改善代谢紊乱,发挥显著的降脂活性( P <0.05 , P <0.01 )。
05 讨论
中药因其复杂性、多样性,显示出广泛药理活性。与合成药物通常针对单一靶点不同,天然产物能够同时作用于多个分子靶标和信号通路,通过协同效应发挥治疗作用。这种多靶点特性使得天然产物在治疗代谢性疾病、心脑血管疾病等复杂疾病方面具有显著优势,可有效克服单靶点药物易产生的副作用及耐药性问题。 化学蛋白质组学技术在天然产物靶标鉴定中的不可替代性,基于 IAA 对蛋白质半胱氨酸残基的选择性标记,结合定量蛋白质组学分析,实现了对天然产物 - 蛋白质相互作用的系统性解析。其主要优势在于它能够直接在 活细胞生理环境下,直接“捕捉”到药物分子与靶标蛋白相互作用,为揭示天然产物复杂而精巧的作用机制提供关键证据。以上方法不仅仅适用于天然产物,对于中药复杂体系同样适用, 目前已利用化学蛋白质组学已揭示了一系列中药复方的靶标蛋白及作用机制,如化湿败毒方通过靶向 PRDX5 发挥抗感染活性,中药蒲地蓝通过靶向 GAPDH 改善急性肺损伤等。长期以来 Res 被报道具有预防癌症、心血管疾病、代谢性疾病等用处,其参与自噬、细胞代谢、抗氧化、抗炎等多种生理过程。传统中药药理学研究的最大难点之一就是发现并确认其药物作用靶点,从而阐释 其药效作用的分子机制。药物靶标蛋白的鉴定对临床应用和现代药物的开发意义重大。本研究在在明确 Res 具有促进棕色化蛋白表达的基础上,利用化学蛋白质组学技术,进一步探究其促进 脂肪棕色化的关键蛋白靶点,并结合细胞热转变分析技术,阐述白藜芦醇在脂质细胞中的剂量和时间依赖效应及其作用机制,为研究改善肥胖及代谢性疾病提供新思路。线粒体,作为细胞的“能量工厂”,线粒体生物合成( mitochondrial biogenesis )是增加线粒体数目和线粒体内容物的过程,促进线粒体 DNA 的复制及表达,进而增加线粒体复合物的合成与组装,改善线粒体能量代谢水平,增强线粒体功能。线粒体数量及功能的增加被认为是白色脂肪棕色化的一个主要特征。其中 UCP1 和 PGC-1 α 是脂肪棕色化调控过程中最核心指征,同时也是线粒体生物合成重要的调节因子。 PGC-1 α 敲除可引起 UCP1 的下调,并阻断线粒体的生物合成。PGC-1 α可以调控棕色脂肪细胞的产热,上调 UCP1 的表达,通过诱导线粒体生物合成将细胞内存储的葡萄糖和脂肪转化为热能,通过热量的形式散发出去。泛醌氧化还原酶核心亚基 S8 ( NDUFS8 )是线粒体复合物 I 的关键亚基,参与线粒体呼吸链中的电子传递和氧化磷酸化过程, NDUFS8 的表达水平直接决定复合物 I 的酶活性,进而调控线粒体 ATP 生成、膜电位维持及 ROS 。 NDUFS8 作为评价线粒体功能的重要指标,在脂肪细胞的线粒体功能中发挥重要作用,其功能异常与多种代谢性疾病密切相关。 研究发现 NDUFS8 在脂肪细胞中的表达水平与肥胖的发生发展存在关联,可能通过影响脂肪细胞的线粒体功能、脂质代谢和能量消耗来调节脂肪组织的生理功能。研究表明, NDUFS8 在肥胖小鼠模型中的表达水平显著降低,且与胰岛素抵抗和脂质代谢紊乱有关。因此, NDUFS8 的激活与脂肪细胞的线粒体功能呈正相关,其活性增加可以显著促进脂肪细胞的能量代谢,减少脂质积累。 NDUFS8 可能是一个潜在的肥胖治疗靶点,通过调节 NDUFS8 的表达或功能,有望改善脂肪细胞的线粒体功能,增强能量消耗,从而达到减轻体重的效果。尽管目前尚无 NDUFS8 靶向药物进入临床,NDUFS8 作 为可靶向亚基,具备以下优势: 1 )其结构明确,可通过基于结构的药物设计开发高选择性抑制剂/激活剂; 2 )功能关键,其激活/抑制可高效促进/阻断靶细胞能量供应; 3 )表达差异显著,为选择性寻找靶细胞提供了可能性。高迁移率族蛋白 1 ( HMGB1 )是一种核蛋白,在细胞应激或损伤时可释放到细胞外,作为损伤相关分子模式分子,激活炎症反应。 HMGB1 通过与 Toll 样受体 4 ( TLR4 )结合, 激活下游的 TNF- α 信号通路, 促进炎症因子如 IL-6 、 TNF- α 等的分泌,从而加剧脂肪组织的炎症。在肥胖状态下,脂肪组织中 HMGB1 的表达和分泌增加,形成慢性低度炎症状态。这种炎症状态不仅影响脂肪细胞的功能,还可能导致胰岛素抵抗等代谢紊乱。抑制 HMGB1 及其激活的 TNF- α 通路,可缓解脂肪炎症,改善肥胖相关代谢紊乱。因此,作为连接损伤、炎症与修复的关键节点,HMGB1 已成为抗炎相关药物研发的重要靶点。近年来,已有多种天然来源的小分子被发现具有 HMGB1 抑制活性,如:甘草酸( Glycyrrhizin )可直接结合 HMGB1 ,改善肝缺血再灌注损伤,丹参酮、表没食子儿茶素没食子酸酯( EGCG )等传统中药成分也显示出 HMGB1 抑制效果。
综上所述,本研究首次系统阐明了白藜芦醇( Res )在 3T3-L1 脂肪细胞中通过直接靶向多个关键信号节点,协同调控 PGC-1 α /UCP1 脂肪棕色化相关能量信号通路,以及炎症信号通路等多条相互关联的信号网络,从而高效诱导脂肪细胞棕色化、改善脂肪炎症干预肥胖。白藜芦醇作为天然产物的明星分子,抑制 3T3-L1 前 脂肪细胞脂滴的沉积,Res 通过靶向 NUDFS8 脂肪细胞线粒体生物合成,促进脂肪棕色化,增加棕色脂肪标志性蛋白 UCP1 、PGC-1 α 表达及 ATP 合成,同时通过靶向 HMGB1 特异性抑制 TNF-α 信号通路,能够有效 缓解脂肪组织慢性炎症,进而改善脂质代谢紊乱并发挥显著的降脂活性。以上发现不仅从多靶点相互作用的角度深刻揭示了白藜芦醇抗肥胖作用的新型分子机制,也为开发以促进脂肪棕色化为精准靶标的下一代抗肥 胖药物奠定了坚实的理论基础。


